【科研新进展】动医学院动物重大疫病病原感染和致病机制研究团队在非洲猪瘟病毒免疫逃逸机制研究中取得重要突破
近日,西北农林科技大学动物医学院动物重大疫病病原感染和致病机制研究团队孙亚妮副教授联合中国农业科学院兰州兽医研究所相关团队在国际学术期刊Autophagy上发表题为“African swine fever virus pE199L, as a mitophagy receptor, suppresses antiviral innate immunity to promote viral replication”的研究论文,首次揭示非洲猪瘟病毒(ASFV)编码的pE199L蛋白作为线粒体自噬受体,通过结构模拟“劫持”宿主自噬系统,降解关键免疫信号分子,从而抑制先天性免疫促进病毒复制。

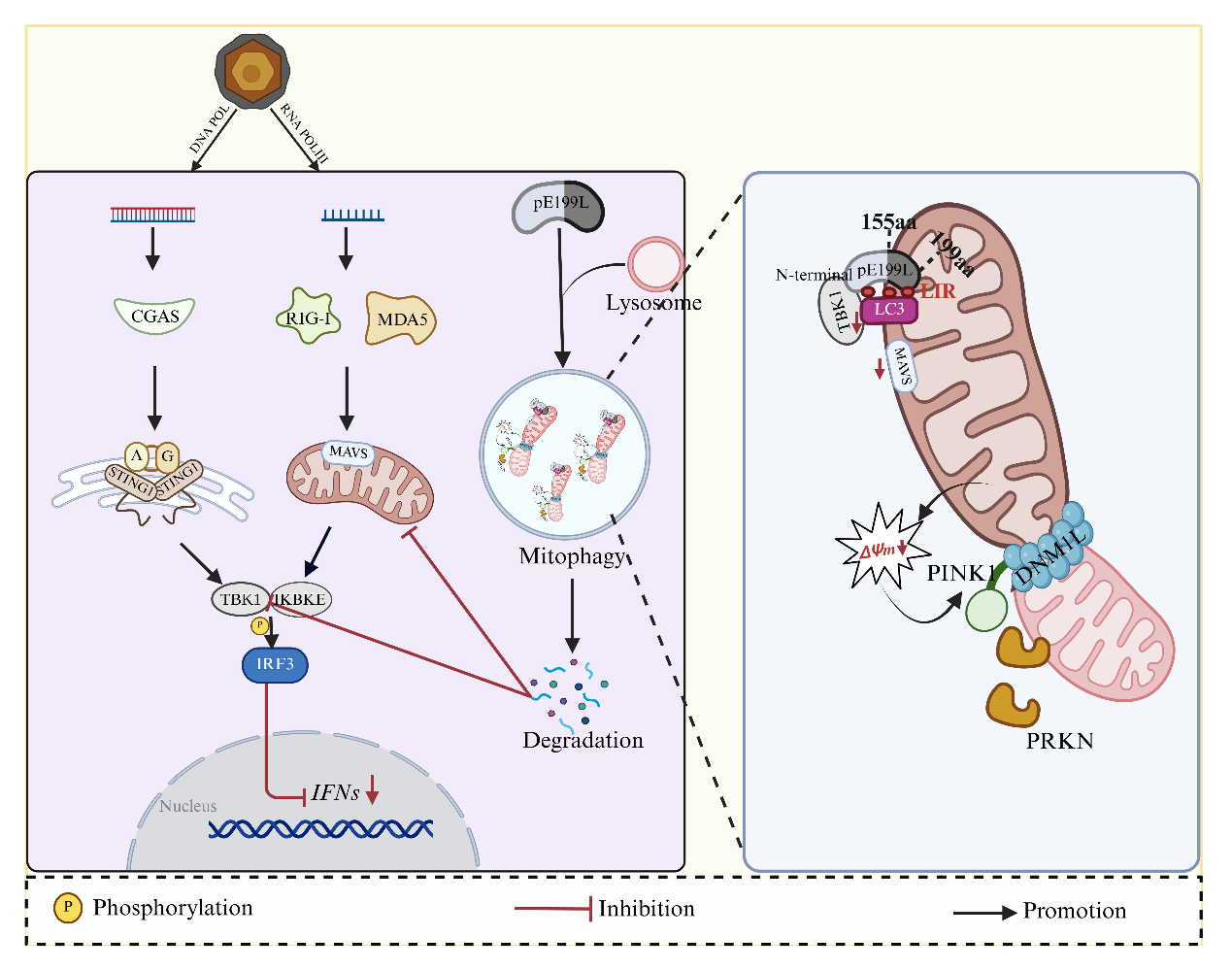
非洲猪瘟是一种急性、高度致死性的动物传染病,目前已在全球多个国家蔓延,给养猪业造成巨大经济损失,由于病毒基因组庞大、结构复杂且缺乏安全有效的疫苗,导致防控工作面临严峻挑战。因此,揭示ASFV复杂的致病机制是研发疫苗和抗病毒策略的关键。该研究团队经过系统攻关发现ASFV编码的pE199L蛋白通过其C端疏水结构域(155-199 aa)精准定位至线粒体,一方面通过促进DNM1L/Drp1蛋白的磷酸化,诱导线粒体过度分裂,促进线粒体自噬;另一方面利用三个保守的LC3结合基序(LIR)直接结合LC3蛋白,进一步诱导线粒体自噬。更为关键的是,研究首次发现pE199L蛋白具备“双重免疫压制”能力,可同时降解TBK1(cGAS-STING通路)和MAVS(RLR-MAVS通路)两种关键抗病毒信号蛋白,显著抑制I型干扰素产生,为病毒复制创造有利条件。
该研究首次鉴定出ASFV编码的线粒体自噬受体,pE199L蛋白不依赖经典的PINK1-PRKN通路,而是通过LIR基序直接“劫持”宿主自噬,实现分子结构模拟。pE199L蛋白可同时靶向TBK1和MAVS,形成“双重”免疫压制策略。此外,团队还构建了LIR突变的重组病毒,从功能上证实了pE199L蛋白在免疫逃逸中的关键作用,为病毒与宿主互作理论提供了基础。
动物医学院在读博士研究生李晓璇为论文的第一作者,孙亚妮副教授和赵钦教授为论文的通讯作者。
该研究得到国家自然科学基金项目、陕西省重点研发计划项目以及国家外国专家项目的资助。
原文链接:https://www.tandfonline.com/doi/full/10.1080/15548627.2026.2654982
编辑:王丹
审核:刘军